随着SOFT和TEXT 研究结果的公布,乳腺癌专家学者在指南中提出了对于不同复发风险人群应采用不同的辅助内分泌治疗策略。那么,哪些患者人群适合卵巢功能抑制(OFS)治疗呢? 本文通过一例绝经前Luminal A型中危复发风险的乳腺癌患者进行卵巢功能抑制剂联合芳香化酶抑制剂(AI)治疗,获得了长期无进展生存的病例分享,探讨OFS的规范应用。
患者绝经前女性,初诊年龄51岁(末次月经时间:2016年4月21日),既往乙肝病毒感染30余年,未行抗病毒治疗,高血压病史2年,规律口服降压药,余无特殊。
患者因“发现左乳肿物4月余”于2016年5月29日我院门诊行乳腺超声检查,结果提示:左乳腺低回声肿块14*19*12 mm,BI-RADS分级5级,考虑乳腺癌?右乳腺片状稍低回声区,BI-RADS分级3级,增生,其他待排除,右乳腺低回声结节,BI-RADS分级3级,局限性增生;双侧腋窝淋巴结可见。
患者于2016年6月6日在我院行“双乳腺肿物切除术+术中冰冻+双乳腺癌改良根治术”。
术后病理学检查结果示:①左乳非特殊型浸润性癌,II级,肿瘤最大径1.1 cm,未见明确血管及神经侵犯。免疫组织化学检查结果显示:癌组织,ER(+,阳性率约90%);PR(+,阳性率约90%);HER2(1+);Ki-67阳性率约8%;②右乳非特殊型浸润性癌,II级,并见导管原位癌成份,肿瘤最大径约2.2 cm,浸润癌灶最大径约0.9 cm,癌旁乳腺组织呈腺病改变。免疫组织化学检查结果显示:浸润癌组织ER(+,约90%);PR(+,约10%);HER2(1+);Ki-67(+,约8%);③乳腺癌根治术大体标本:左乳腺乳头非特殊类型浸润性癌(II级),缺损区见少许癌组织残留,切缘未见癌累及;腋窝淋巴结(1/16)转移癌。免疫组织化学检查结果显示:ER(+,>95%);PR(+,>95%);HER2阴性,Ki-67(+,约10%);P120(+);CK5/6(-);E-Cadherin(+)。右乳腺缺损区未见癌,乳头及切缘未见癌累及;腋窝淋巴结20枚,未见癌累及。
术后诊断:①左乳腺非特殊型浸润性癌II级(pT1cN1M0、IIA期 Luminal A型)②右乳腺非特殊型浸润性癌II级(pT1N0M0、IA期、HER2阴性、激素受体阳性)③乙肝病毒携带④高血压病。
辅助放化疗:2016年6月24日~2016年10月25日,行3周期FEC(氟尿嘧啶750 mg D1 +吡柔表星60 mg+环磷酰胺750 mg D1)序贯3周期T(紫杉醇脂质体260 mg D1)方案化疗,过程顺利,患者不接受放疗。
辅助内分泌治疗:2016年11月开始行戈舍瑞林联合来曲唑内分泌治疗至今, 按时定期复查。
《中国早期乳腺癌卵巢功能抑制临床应用专家共识(2016版)》中,推荐高复发风险的绝经前激素受体阳性乳腺癌患者接受含 OFS 的内分泌治疗,中危患者应考虑使用,低危患者不推荐使用。2018版OFS共识与2016版相比,将OFS的获益人群由高危和部分中危更新为中危和高危,强调了中危患者OFS治疗的获益。
图1《中国早期乳腺癌卵巢功能抑制临床应用专家共识》2016版及2018版OFS的推荐人群
这一更新主要基于2018年《新英格兰医学杂志》(N Engl J Med)发表的SOFT研究8年随访结果,研究进一步证实了OFS可使整体人群获益。回顾该研究的历程,2014年公布的5年随访结果显示,OFS联合他莫昔芬对比他莫昔芬单药在总体人群中没有显著获益;但在接受化疗的亚组中,与他莫昔芬单药组(78.0%)相比,OFS联合AI组(85.7%)和OFS联合他莫昔芬组(82.5%)的5年无乳腺癌生存绝对获益分别为7.7%和4.5%,复发风险分别降低了35%(HR=0.78,95%CI:0.60~1.02)和22%(HR=0.65,95%CI:0.49~0.87);在年龄<35岁的年轻患者中,与他莫昔芬单药组(67.7%,95%CI:57.3~76.0)相比,OFS联合AI组(83.4%,95%CI:74.9~89.3)和OFS联合他莫昔芬组(78.9%,95%CI:69.8~85.5)的5年无乳腺癌生存绝对获益分别为15.7%和11.2%。在未化疗亚组中,3个治疗组的无乳腺癌生存率均>95%。
2018年N Engl J Med发表的SOFT 研究8年随访结果进一步证实了整体人群的获益,OFS联合他莫昔芬较他莫昔芬单药组显著提高了无病生存率(83.2%对78.9%,HR=0.76,95%CI:0.62~0.93, P=0.009)及总生存率(93.3%对91.5%,HR=0.67,95%CI:0.48~0.92)。OFS联合AI相较于他莫昔芬单药组在整体人群中显著提高了无病生存率(85.9%对78.9%,HR=0.65,95%CI:0.53~0.81)。其中,未化疗亚组和化疗亚组患者的无疾病生存率趋势未见异质性。化疗亚组中OFS联合他莫昔芬相较于他莫昔芬单药组,随访8年的无病生存率分别为76.7%和71.4%,绝对获益率为5.3%;未化疗亚组,8年的无病生存率分别为90.6%和87.4%,绝对获益率为3.2%。在年龄<35岁的人群中,OFS联合他莫昔芬相较于他莫昔芬单药组随访8年的无病生存率分别为73%和64.3%,绝对获益率为8.7%。
分析本病例,患者手术前仍有月经,属于绝经前女性患者,术后病理显示仅1个腋窝淋巴结阳性,为中度复发风险患者。根据指南的推荐,给予患者卵巢功能抑制剂(戈舍瑞林)治疗。
临床实践中OFS应联合AI或是他莫昔芬,哪种联合方案更佳?2014年发布的SOFT和TEXT两项研究结果均比较了OFS联合AI组及OFS联合他莫昔芬组的疗效。SOFT研究中,两组的5年无病生存率分别为91.1%和87.3%,绝对获益率为3.8%(HR=0.72,P<0.001);TEXT研究中,两组的5年无病生存率分别为92.8%和88.8%,绝对获益率为4%(HR=0.66,P<0.001);在接受化疗患者中,OFS联合AI组较联合他莫昔芬组的远处复发率降低了2.6%(TEXT研究)和3.4%(SOFT研究)。
2018年N Engl J Med发表的最新SOFT和TEXT研究结果再次证实,OFS联合AI可显著提高整体人群的预后。与OFS联合他莫昔芬组相比,OFS联合AI组显示出无病生存持续的改善,8年无病生存率分别为82.8%和86.8%(HR=0.77,95%CI:0.67~0.90,P=0.0006),绝对获益为4%;同时可减少远处复发,8年无远处复发率分别为89.7%和91.8%(HR=0.80,95%CI:0.65~0.96),绝对获益为2.1%;HER2阴性患者(占总人群的86%)中,OFS联合AI可改善所有亚组的疾病预后;而HER2阴性且高风险需接受化疗的患者中,OFS联合AI治疗组获得了显著的临床获益,在TEXT和SOFT研究中,无病生存绝对获益率分别为6.9%和9.2%,无远处复发间期绝对获益分别为5%和7%。
2018年欧洲肿瘤内科学会(ESMO)年会上公布的HOBOE-2研究同样也证实了OFS联合AI显著优于OFS联合他莫昔芬,5年无病生存率绝对获益达7.8%(HR=0.72,95%CI:0.48~1.07,P=0.06)。
综上所述,针对本例中危患者,我们给予戈舍瑞林+来曲唑内分泌治疗。
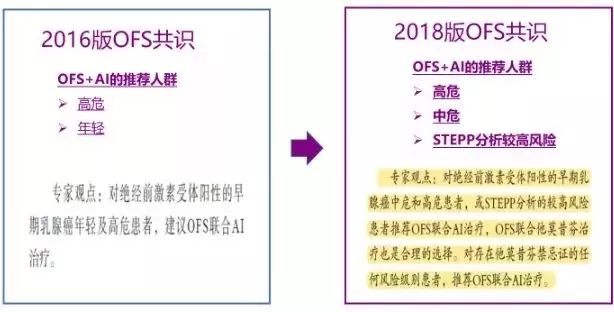
图2《中国早期乳腺癌卵巢功能抑制临床应用专家共识》2016版及2018版OFS联合方案的推荐
关于促性腺激素释放激素激动剂(GnRHa)在绝经前乳腺癌患者治疗中的最佳疗程,目前尚无明确定论。既往关于GnRHa用于绝经前乳腺癌辅助治疗的重要临床研究采用了2、3或5年的OFS疗程,其中,SOFT/TEXT研究采用5年OFS治疗,目前尚缺乏不同GnRHa治疗疗程的对比研究。《中国早期乳腺癌卵巢功能抑制临床应用专家共识》(2018版)建议辅助GnRHa治疗的疗程为5年。
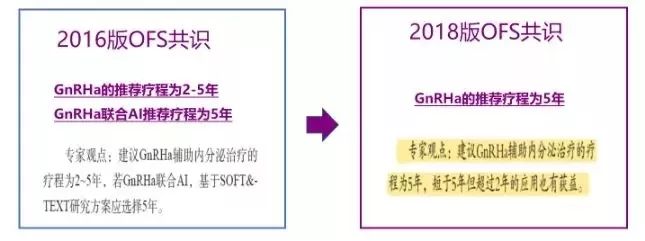
图3《中国早期乳腺癌卵巢功能抑制临床应用专家共识》2016版及2018版GnRHa的推荐疗程
本例患者已使用戈舍瑞林治疗3年余,我们建议患者在可耐受不良反应的前提下,继续使用最多5年,同时给予每6月一次唑来膦酸治疗。
?
通过对文献的回顾和重要研究的梳理,同时遵循OFS专家共识,本例患者在手术、化疗后,使用GnRHa戈舍瑞林进行OFS治疗,获得了长期无进展生存。由此可见,GnRHa是绝经前乳腺癌患者有效的OFS选择,在临床实践中,我们应遵循循证医学证据,紧随学术前沿热点,并针对不同的患者,采用个体化精准治疗,从而改善患者生存。
?
参考文献:
[1] 中国抗癌协会乳腺癌专业委员会. 中国早期乳腺癌卵巢功能抑制临床应用专家共识(2016年版).中国癌症杂志,2016,26(8):712-718.
[2] 中国抗癌协会乳腺癌专业委员会. 中国早期乳腺癌卵巢功能抑制临床应用专家共识(2018年版).中国癌症杂志, 2018, 28(11): 871-880.
[3] FRANCIS P A, REGAN M M, FLEMING G F, et al. Adjuvant ovarian suppression in premenopausal breast cancer[J].N Engl J Med,2015,372(5):436-446.
[4] FRANCIS P A, PAGANI O, FLEMING G F, et al. Tailoring adjuvant endocrine therapy for premenopausal breast cancer[J]. N Engl J Med 2018; 379(2): 122-137.
[5] PAGANI O, REGAN M M, WALLEY B A, et al. Adjuvant exemestane with ovarian suppression in premenopausal breast cancer[J]. N Engl J Med, 2014, 371(2): 107-118.
[6] PERRONE F, LAURENTIIS M D, PLACIDO S D, et al. The HOBOE-2 multicenter randomized phase 3 trial in premenopausal patients with hormone-receptor positive early breast cancer comparing triptorelin plus either tamoxifen or letrozole or letrozole + zoledronic acid[J]. Ann Oncol, 2018, 29(suppl 8).Epub ahead of print.
审批编号:CN-43842
有效日期至:2021-1-13





 京公网安备 11010502033352号
京公网安备 11010502033352号